Durch künstliche Intelligenz zum perfekten Medikament
Eine Deep-Learning-Plattform für medizinische Chemiker zur schnelleren und genaueren Vorhersage von Bindungsaffinitäten und daraus resultierendem Design von Arzneimitteln – das will das Start-up Celeris Therapeutics aus Graz noch dieses Jahr zur Marktreife entwickeln.

80 % der pathogenen Proteine im Körper gelten bislang als untherapierbar. Das Celeris-Team will diese durch neuartige Methoden im Deep Learning für Arzneimittel zugänglich machen. Hierfür wird auf bislang unkonventionelle, aber äußerst vielversprechende Repräsentationen von Molekülen in Form von Graphen gesetzt. Das Design der Arzneimittel mittels computerbasierender Methoden soll einen Denkanstoß für medizinische Chemiker geben und neue, synthetisierbare Moleküle, die als Arzneimittel wirken können, vorschlagen. Die beiden Gründer Christopher Trummer und Jakob Hohenberger erläutern ihre Technologien und die Entwicklungsziele.
CHEManager: Künstliche Intelligenz ist ein dynamisches Forschungsfeld, auf dem sich viele renommierte und finanzstarke Unternehmen tummeln. Können Sie hier mitmischen?
Christopher Trummer: Wir haben ganz klare Visionen und eigene Technologien. In den letzten Dekaden haben große Pharmafirmen unglaubliche Mengen an Daten produziert, sei es in der Forschung oder auch in den Bereichen Produktion und Regulatorik. Eine notwendige Konsequenz ist es, diese Daten nun sinnvoll zu verwerten, um etwaige Vorhersagen treffen zu können. So werden Kosten und Entwicklungszeiten gesenkt, was nicht nur im Interesse der Pharmaindustrie, sondern im Interesse der gesamten Menschheit ist. Und trotz einiger großer Player am Markt ist das Potenzial enorm, und auf mittel- und langfristige Zeit ist künstliche Intelligenz in der Pharmabranche einer der Wachstumsmärkte. Industrieunternehmen und Investoren klopfen bereits bei uns an. Das zeigt uns, dass es in diesem Markt noch ein großes Potenzial für weitere Entwicklungen gibt.
Aber was unterscheidet Celeris von Mitbewerbern?
Jakob Hohenberger: Die medizinische Chemie im Bereich des Deep Learning für Drug Discovery wurde in den letzten Jahren insbesondere durch Repräsentationen von Molekülen forciert, die auf Basis einer Syntax funktionieren. Diese sogenannten SMILES-Repräsentationen von chemischen Reaktionen erzeugen einen großen Overhead und sind aus unserer Sicht zu ungenau. Wir sehen die Welt der Moleküle, sei es bei Liganden oder Proteinen, mit unserem Ansatz zum Deep Learning in einer dreidimensionalen Struktur und geodesisch. Das ermöglichen uns Graphen-Repräsentationen. Dieser innovative Ansatz lässt genauere und schnellere Vorhersagen zu.
Welche Einsatzmöglichkeiten hat Ihre Plattform im Bereich Drug Discovery?
C. Trummer: Das ist das Schöne an unserem Ansatz, er ist recht generisch anwendbar. Wir haben ein großes Portfolio an möglichen Anwendungen, wie etwa Virtual Screening mittels Deep Learning, de-novo-Drug-Design mittels voll-generativen Ansätzen, die Vorhersage von Protein-Protein-Interaktionen oder das Finden von sogenannten Off-Targets.
Wir wollen also neuartige Moleküle vorhersagen und medizinische Chemiker bei ihrer Auswahl an möglichen Wirkstoffen für nasschemische Versuche unterstützen, respektive neue Einblicke gewähren.
Und die Plattform soll direkt den Kunden zur Verfügung stehen?
J. Hohenberger: Genau. Wir sehen auch für medizinische Chemiker die Notwendigkeit, sich intensiver mit der unerforschten chemischen Welt auseinanderzusetzen, und das funktioniert mit Deep Learning. Das wurde mehrfach validiert, etwa mit Assessments zu Löslichkeit, Synthetisierbarkeit und Drug Likeness. Diese Welt soll Pharma einfach zugänglich gemacht werden und insbesondere für die Forschenden auf diesem Gebiet in einer intuitiven Lösung, die einfach zu bedienen ist, Anwendung finden.
Woran arbeiten Sie denn aktuell?
C. Trummer: Wir betätigen uns in einem stark forschungsgetriebenen Feld. Daher widmen wir den Hauptteil unserer Arbeit technologischen Themen und der Weiterentwicklung unserer Deep-Learning-Methoden. Celeris hat bereits erste Traktion am Markt gewinnen können, und noch in diesem Jahr soll die Plattform als SaaS-Modell global vertrieben werden. Da wir an der Schnittstelle von gefragten Technologien sitzen, haben wir entsprechend hohe Personalaufwendungen. Diese wollen wir mit weiteren externen Investoren und Förderungen abdecken.

Zur Person
Jakob Hohenberger ist COO und Mitgründer von Celeris Therapeutics. Er studierte Informatik an der Technischen Universität Graz und absolvierte Programme in Fintech und Blockchain Strategy an der Saïd Business School, University of Oxford. Als Serial Tech-Entrepreneur bringt er weitreichende Expertise in diversen Bereichen, von Softwareentwicklung über Branding und Vertrieb bis Finanzen, ein. Getrieben von den Entwicklungen in der pharmazeutischen Industrie und den Fortschritten in künstlicher Intelligenz möchte er sein Skillset nutzen, um echte Werte für Menschen zu schaffen.
Zur Person
Christopher Trummer ist CEO und Mitgründer von Celeris Therapeutics und vereint die Bereiche Bioinformatik und Wirtschaft durch seine beiden entsprechenden Master-Abschlüsse an der Technischen Universität Graz bzw. der IUBH Internationale Hochschule. Er begann seine Laufbahn 2017 bei Fresenius Kabi und konnte vor allem in seiner knapp zweijährigen Tätigkeit als Business Developer im Bereich Enzyme und Drug Discovery beim Wiener Unternehmen Innophore nicht nur ein weitreichendes Netzwerk, sondern auch entscheidendes Technologieverständnis aufbauen.
 Business Idea
Business Idea

Better Drugs Faster
Durch Patentausläufe und rückläufige Umsatzzahlen sowie immer anspruchsvollere und kostspieligere F&E-Prozesse steht die pharmazeutische Industrie unter einem Veränderungsdruck.
Celeris fokussiert sich auf geometrisches Deep Learning als Technologie und entwickelt auf dieser Basis eine Software-as-a-Service (SaaS)-Plattform, um die Lücke zwischen medizinischer Chemie und den letzten Erkenntnissen aus der Chemo- und Bioinformatik zu schließen.
Durch diesen Brückenschlag können die enormen Kosten der Medikamentenentwicklung von bis zu 2,5 Mrd. USD und die langen Entwicklungszeiten von bis zu 15 Jahren drastisch reduziert werden.
Das Produkt: skalierbare Web-Plattform
Die Plattform Xanthos ist eine cloudbasierte Web-Anwendung, in der Projekte und Biomoleküle verwaltet werden. Die Projekte werden in Workflows im Team bearbeitet. Sie deckt die Wertschöpfung von Virtual Screening und Target Deconvolution bis De-novo-Design von synthetisierbaren, niedermolekularen Verbindungen und Labor-Feedback-Schleifen ab.
Durch die Vorhersage von Protein-Protein-Interaktionen sowie einem Modul für Protac Linker Design richtet sich die Plattform auch an Unternehmen, die mit dem vielversprechenden Arzneimittelkonzept der Targeted Protein Degradation (z. B. Proteolysis Targeting Chimerae (Protacs)) arbeiten.
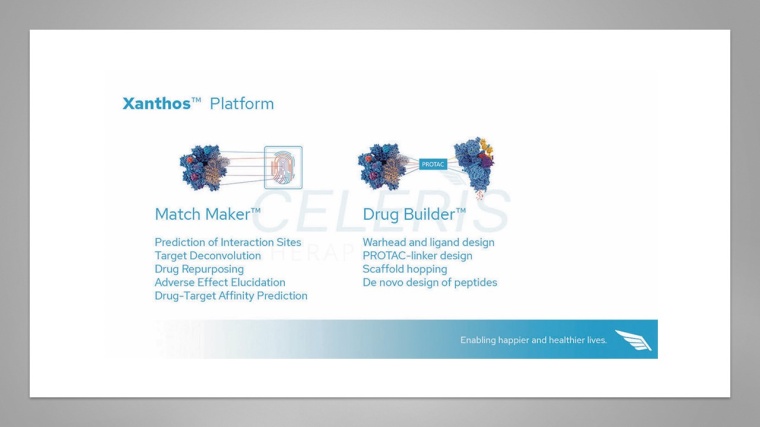
Die Module: Match Maker und Drug Builder
Xanthos besteht aus Match Maker und Drug Builder. Die Aufgabe des Match Maker ist es, Interaktionen anhand von 3D-Strukturen sowohl zwischen Protein-Protein als auch Protein-Ligand vorherzusagen. Hierdurch werden Protein-Protein-Interaktionen (PPIs), Drug-Target Interaktionen (DTIs) und Off-Targets bestimmt.
Der Drug Builder lernt aus diesen Vorhersagen, um mittels Deep Learning neue Moleküle zu generieren. Am Ende des Workflows wird ein Bericht mit allen Informationen erstellt, der zum Review an das Team geschickt wird.
 Elevator Pitch
Elevator Pitch

Meilensteine und Roadmap
Celeris wurde im Herbst 2020 von Jakob Hohenberger und Christopher Trummer gegründet und hat seinen Sitz in Graz. Die Gründer bringen ihre Expertise in Biotechnologie, Wirtschaftsinformatik und Software Engineering ein, dazu beschäftigt das Start-up derzeit noch einen mathematischen Physiker, einen medizinischen Chemiker, einen Senior Data Scientist und einen Junior Deep Learning Engineer.
Während das Team das letzte Jahr dafür aufgewendet hat, um die Technologie zu entwickeln, beginnt Celeris nun seinen eigentlichen Expansionskurs.
Die End-to-end Plattform ermöglicht es medizinischen Chemikern, Arzneimittel zu designen und so unentdeckten chemischen Raum zu erforschen. Die einzelnen Pipelines werden aktuell in eine Web-Applikation mit durchgehendem Workflow integriert. Das Produkt des Grazer Start-ups, die Xanthos Plattform, enthält zwei Module:
Der Xanthos Match Maker ermöglicht Deep Learning-basierendes Virtual Screening, Off-Target Bestimmungen, Drug Repurposing und Bestimmungen von Protein-Protein-Interaktionen (PPIs). Match Maker zeigt eine überdurchschnittliche Performance und Genauigkeit in der Bestimmung von biomolekularen Interaktionen.
Der Xanthos Drug Builder ist ein vollgeneratives System zum Arzneimitteldesign und hebelt die Resultate des XMM. Am Ende des Workflows startet eine nasschemische Feedback-Schleife, welche Ergebnisse evaluiert, Algorithmen verbessert und die optimalen Resultate liefert. Die Plattform wird als Cloud-Lösung dank Unterstützung von AWS Activate, der Plattform für Start-ups von Amazon Web Services, angeboten werden.
Roadmap:
2020
- Gründung der Celeris Therapeutics GmbH in Graz, Österreich
- Aufbau und Entwicklung der Technologie des Deep Learning für Drug Discovery
- Funding durch die Amazon-Start-up-Plattform AWS Activate
2021
- Ende Januar: Abschluss der aktuellen Finanzierungsrunde
- September: nächste Finanzierungsrunde geplant
- Ende 2021: Product Launch über AWS Activate
- Personalerweiterung um 8 FTEs






