Elektrifizierung der Bioökonomie
B.fab macht Chemikalien und Proteine aus CO2 und erneuerbarem Strom zugänglich
Die herkömmliche Biotechnologie nutzt in der Regel Zucker als Rohstoff. Das Start-up B.fab möchte dies ändern, indem es mikrobiellen Zellen beibringt, auf Formiat, also Ameisensäure, zu wachsen. Genauer noch, die Dortmunder Firma kombiniert Elektrochemie mit Biotechnologie, um damit den effiziensten Weg zur Umsetzung von CO2 in Produkte zu nutzen. Gegründet wurde B.fab von Frank Kensy und Arren Bar-Even in Partnerschaft mit dem Firmenentwickler B.value.
Das Start-up ist eine Ausgründung aus dem Max Planck Institut für molekulare Pflanzenphysiologie (MPIMP), wo Arren Bar-Even als unabhängiger Gruppenleiter tätig ist.
CHEManager: Herr Kensy, was war die Motivation für die Gründung?
Frank Kensy: Inspiriert durch die frühen Arbeiten von LanzaTech und Covestro wollten wir einen neuen biotechnologischen Weg zur CO2-Verwertung beschreiben. Einerseits gibt es in der Biologie schon einige natürliche Stoffwechselpfade, die CO2 verwerten, andererseits wußten wir, dass die schnellen Entwicklungen im Bereich der Synthetischen Biologie ein riesiges Potenzial für die Ausgestaltung neuer Herstellungsrouten und Produkte bietet. Des Weiteren hatte Arren Bar-Even in seiner Promotion bereits die Grundlagen für einen neuen, synthetischen Stoffwechselweg gelegt. 2018 war es dann an der Zeit, die Grundlagen in die Applikation und kommerzielle Verwertung zu überführen und mit B.fab zu verwerten.
Welche Probleme lösen Sie mit B.fab konkret?
F. Kensy: Wir versuchen die Produktionsverfahren für Proteine und Chemikalien auf eine nachhaltige Basis zu stellen, indem wir CO2 als Rohstoff verwenden. Um unsere Klimaziele zu erreichen, müssen wir CO2-Emissionen drastisch reduzieren. Aber nicht alle Industrien können von heute auf morgen umgerüstet werden. Wir bieten an, aus den Emissionen Produkte zu formen. Gleichzeitig erhalten wir damit einen günstigen Rohstoff, den wir mit erneuerbarem Strom aufwerten und in Produkte wie Biopolymere oder Futtermittel wandeln.
Welche Herausforderungen gab es bei der Gründung?
F. Kensy: Einerseits mussten wir die Rechte an den Patenten für die Firma sichern und andererseits brauchten wir die erste Finanzierung, um loszulegen. Nach der Bewältigung einer riesigen Menge an Bürokratie und einigen Monaten Verzögerung konnten wir uns die Patentrechte sichern. Hier ist hervorzuheben, dass deutsche Behörden eindeutig nicht kompatibel mit Start-ups sind. Ausländische Behörden, mit denen wir zu tun hatten, agieren hier wesentlich Gründer-freundlicher. Da muss sich dringend etwas ändern! Die zweite große Hürde, war die Anschubfinanzierung. Hier hatten wir etwas Glück, dass wir B.value als Gründer mit an Bord hatten. Die nächste Finanzierungsstufe, das Seed-Investment, ist jedoch in Deutschland für Firmen wie unsere äußerst schwierig. Deutsche Investoren agieren sehr risikoavers. Ich befürchte, dass dies kein guter Nährboden für disruptive Technologien ist.
Wo steht die Firma heute und was sind die nächsten Schritte?
F. Kensy: Technologisch gesehen haben wir den Proof-of-Principle, dass unser Stoffwechselweg funktioniert, mit den ersten zwei Bakterien, Escherichia coli und Cupriavidus necator, erbracht. Dies weiten wir nun auf Hefe aus. Des Weiteren nehmen wir nun die ersten Produktsynthesen in den Bakterien vor. Danach soll es schnell in die Prozessetablierung und Weiterentwicklung im Labormaßstab gehen. Während die grundlegende Klonierung des Stoffwechselwegs noch am MPIMP stattfindet, übernimmt B.fab die weitere Stammoptimierung und die Prozessentwicklung. Um voll Durchstarten zu können, müssen wir aber noch die Seed-Finanzierung abschließen. Die Signale der Investoren sind sehr positiv, doch fehlt in Deutschland der Mut. Daher sprechen wir derzeit mit europäischen und amerikanischen Investoren.
Was sind ihre langfristigen Ziele mit B.fab?
F. Kensy: Wir wollen mit B.fab die Formiat-Bioökonomie am Markt etablieren und unsere Plattform möglichst breit implementieren.
ZUR PERSON
Frank Kensy, Gründer und CEO. hat an der RWTH Aachen Bioverfahrenstechnik studiert und anschließend promoviert. Nach Aufenthalten in Spanien und Brasilien begann er seine Karriere als Gruppenleiter der Fermentation bei Rhein Biotech und sammelte umfassende Erfahrungen in der Bioprozessentwicklung. Zwischen 2005 und 2015 war er Gründer und Geschäftsführer von m2p-Labs und entwickelte die Firma zu einem führenden Anbieter von Mikrobioreaktoren (BioLector/RoboLector). Anschließend war er als freier Berater im Bereich des Innovationsmanagements tätig. Seit März 2018 ist er Gründer und Geschäftsführer von B.fab und baut die Firma auf.
Arren Bar-Even, Gründer und wissenschaftlicher Beirat, hat seinen Master-Abschluss in Bioinformatik am Weizmann Institute of Science in Rechovot, Israel, abgeschlossen. Anschließend arbeitete er vier Jahre als F&E-Leiter bei SegaChem an einer neuen Generation von Insektenschutzmitteln. Von 2009 bis 2012 kehrte er ans Weizmann Institute of Science zurück, um seine Promotion in Biochemie über das Thema Design-Prinzipien von metabolischen Stoffwechselwegen anzufertigen. Seit dem Jahr 2015 ist er am Max Planck Institut für molekulare Pflanzenphysiologie in Golm tätig, wo er als unabhängiger Gruppenleiter mit ca. 30 Forschern das Thema “Systems and Synthetic Metabolism” vertieft.
BUSINESS IDEA
Formiat-Bioökonomie
B.fab ist spezialisiert auf die effiziente Verwertung von Kohlendioxid (CO2) und Wasserstoff (H2) aus regenerativer Energie in biotechnologischen Wertschöpfungsketten. Formiat ist dabei der zentrale Energiespeicher für die gasförmigen Ausgangssubstrate (CO2+H2) und wird als neues unbegrenzt verfügbares Substrat für die Fermentation eingesetzt.
Der flüssige Aggregatzustand des Substrats Formiat lässt eine gute Lagerung und den unproblematischen Transport von dezentralen Produktionsstandorten zu biotechnologischen Produktionsstätten zu. Über moderne Werkzeuge der synthetischen Biologie werden neue Stoffwechselwege basierend auf dem Substrat Formiat in etablierte, aerobe Produktionswirte wie E.coli und Hefen integriert. Pathway-Design ermöglicht es, die effizientesten Reaktionswege in dem Produktionsstamm zu gestalten und somit die eingesetzte Prozessenergie mit wenig Verlust in das Produkt zu überführen. Die Verwendung von herkömmlichen, aeroben Produktionswirten garantiert eine schnelle und gezielte molekularbiologische Veränderung der Stämme und deren Stoffwechselwege. B.fab verfügt zudem über langjährige Erfahrung im Bereich der hochparallelen und automatisierten Bioprozessentwicklung und im Scale-up von Bioprozessen.
Mit der Formiat-Bioökonomie stellt das Start-up eine neue, energie- und zugleich kosteneffiziente Plattformtechnologie für KMUs und die Industrie bereit.
Die Vorteile auf einen Blick:
- kostengünstiger und unbegrenzt verfügbarer Rohstoff (CO2)
- Formiat speichert CO2 und H2 in flüssiger Form
- niedriger Landflächenbedarf durch hohe Energieeffizienz
- hohe Prozessflexibilität durch aeroben, mikroaerophilen oder anaeroben Betrieb
- schnelle Entwicklungszeiten durch Einsatz etablierter Produktionsorganismen
- breites Produktspektrum durch synthetische Biologie
B.fab wird Plattformstämme mit dem Basisstoffwechselweg zur Verwendung bei den Kunden anbieten oder aber im Auftrag der Kunden die Implementierung der Produktsynthese und der Prozessentwicklung übernehmen. Das Start-up bietet ebenfalls den Prozess als Technologielizenz weltweit an und hilft beim Technologietransfer. Die Nutzung von synthetischer Biologie wird das Produktspektrum stetig erweitern.
ELEVATOR PITCH
Meilensteine und Roadmap
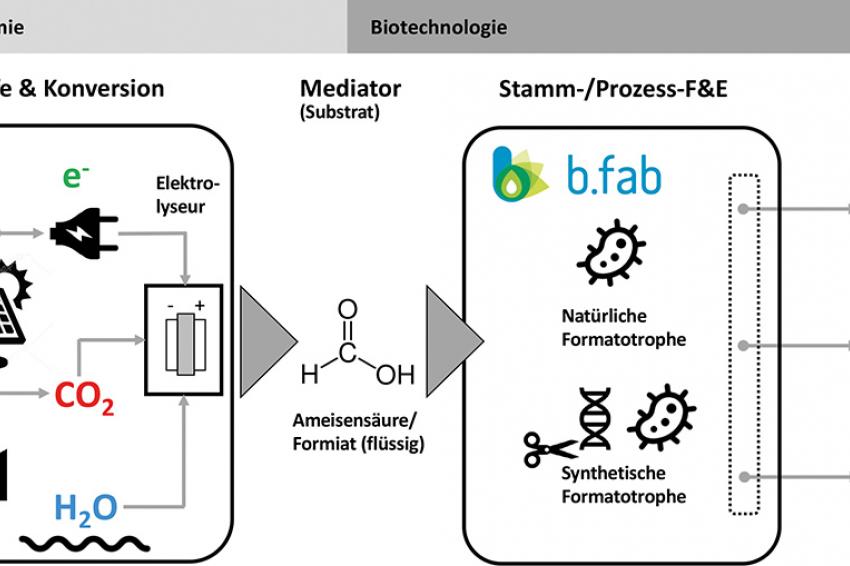
B.fab elektrifiziert die Bioökonomie durch Kombination von künstlicher Photosynthese (CO2-Reduktion im Elektrolyseur) und synthetischer Biologie (Einsatz synthetischer Stoffwechselwege). Dieser Ansatz besitzt eine um den Faktor 10 bis 40 höhere Energieeffizienz als bestehende biotechnologische Prozesse und Wertschöpfungsketten. Durch den Einsatz von Mikrobioreaktoren und Laborautomatisierung will B.fab die internen Prozesse in der Stamm- und Prozessentwicklung weiter beschleunigen und ein Höchstmaß an Daten und Output erzeugen.
MEILENSTEINE
2018
- Gründung in Dortmund
- Teilnahme am StartUP InnoLab der TU Dortmund
- Abschluss der Pre-Seed Finanzierungsrunde mit B.value
- Start des Horizon2020-Projekts eforfuel zur Produktion von Isobuten und Propan aus CO2 (B.fab als Beirat)
- Start des Projektes CO2PERATE zur CO2-Verwertung in Formiat durch Catalisti in Flandern (B.fab als Beirat)
- Proof-of-Principle mit Bakterien
2019
- Abschluss des exklusiven Patent-Lizenzvertrags
- 3. Preis für “Best CO2 Utilisation 2019” auf der “7th Conference on Carbon Dioxide as Feedstock for Fuels, Chemistry and Polymers” von Nova-Institut und Covestro.
- 2. Preis beim Greentech Innovation Call, Business Metropole Ruhr
- Erfolgreiche Begutachtung eines BMBF-Antrags CO2-WIN für ein Verbundvorhaben mit 7 Partnern zur Entwicklung der Formiat-Bioökonomie
ROADMAP
2019
- Abschluss der Seed Finanzierung
- Anstellung weiterer Mitarbeiter
- Bezug und Einrichtung eigener Labore
2020
- Start des BMBF-Projekts CO2-WIN mit 7 Partnern
- Vollständige Automatisierung der internen Prozesse
- Akquise und Abschluss des ersten Service-Auftrags für Kunden
- Proof-of-Principle mit Hefe erbracht
- Erste Produktsynthese in Bakterien etabliert
- Teilnahme an weiteren BMBF- und EU-F&E-Ausschreibungen
2021
- Erste Produktsynthese in Hefe
- Prozessoptimierung im Labormaßstab (2-10L)
- Angebot der Plattform-Stämme für externe Kunden
- Transfer des Prozesses in den Pilotmaßstab
CHEManager Innovation Pitch ist nicht nur eine Präsentationsplattform für Start-ups in den monatlichen Printausgaben des CHEManager, sondern auch auf einer eigenen Online-Plattform. Besuchen Sie www.chemanager-innovationpitch.de und finden Sie weitere Start-ups aus der Chemiebranche und Informationen über unsere Sponsoren, die den CHEManager Innovation Pitch unterstützen.