Wachstumsstrategien für Pharma- und Biotechfirmen
Wachstum versus Schlankheitskur
Die aktuelle Stimmung in der Pharmaindustrie ist und bleibt geprägt vom steten Wunsch nach mehr Wachstum aus eigener oder externer Innovationsleistung. Ein probates Mittel hierfür ist die Entwicklung neuer Therapien für Krankheiten mit bisher unzureichenden Behandlungsmöglichkeiten. Die Branche zeichnete sich im Jahr 2014 vor allem dadurch aus, sich zu verschlanken bzw. den Therapiefokus zu schärfen. Es war ein Jahr der Übernahmemeldungen.
Die amerikanische Merck verkaufte ihre Consumer Sparte an Bayer; Abbott gab einen Teil seines Generikageschäftes ab; GSK und Novartis haben Onkologie gegen Vakzingeschäft getauscht und Roche verstärkte sich durch den Zukauf von Technologien für die personalisierte Medizin. Nach erfolgreicher Abwehr des Zusammenschlusses mit Abbott, gelang Shire mit der Übernahme des Specialty-Pharma-Unternehmens NPS ein weiterer Schritt in der konsequenten Umsetzung der Nischen- und Orphan-Strategie.
Doch es gibt auch Beispiele für organisches Wachstum und erfolgreiche Lizensierungsstrategien. Mit über 40 Neuzulassungen durch die FDA war das Jahr 2014 im historischen Vergleich ein Rekordjahr. Rekordverdächtig sind auch die Zuwachsraten im Bereich der Biotechfirmen, insbesondere bei den Börsengängen, den sog. Initial Public Offerings (IPOs). Auch das Jahr 2015 lässt auf ein Fortsetzen des Wachstumstrends hoffen.
Hohe Anzahl an Opportunitäten
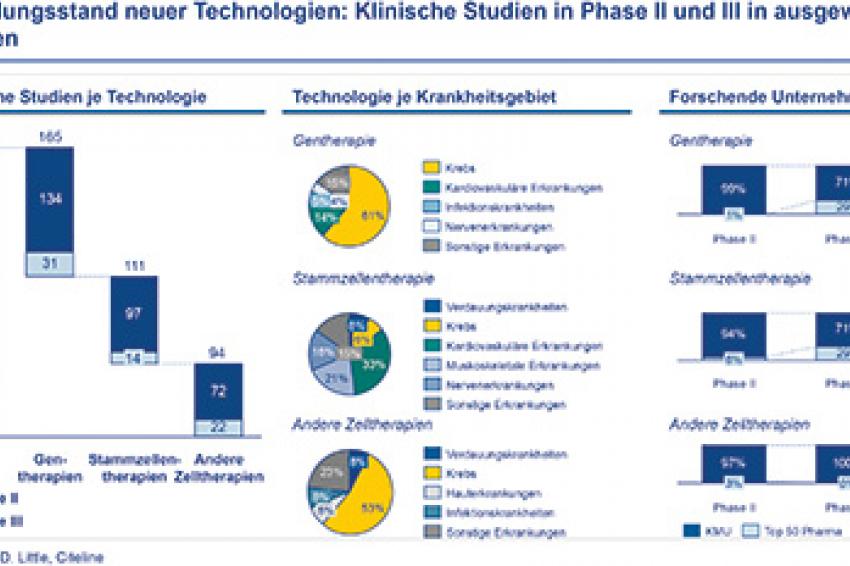
Auch wenn der Nasdaq-Biotech zuletzt primär nur durch wenige große Werte mit etwa 40% wachsen konnte, sind die Forschungspipelines gut gefüllt. Eigentümer vielversprechender Kandidaten sind häufig kleinere Biotech- und Specialty-Firmen. Big Pharma hat sich in den letzten Jahren vor allem mit Themen der Effizienzsteigerung in der Forschung beschäftigt und vorwiegend auf bekannte Technologien und Targets in den bereits wettbewerbsintensiven Indikationsgebieten gesetzt. Unterdessen waren die kleineren, manchmal sogar familiengeführten Unternehmen risikobereiter und sicherten sich einen relativen Innovationsvorsprung. Dieser Innovationsvorsprung zeigt sich sowohl in der Anzahl der fortgeschrittenen Entwicklungsprojekte, als auch in der Bandbreite der fokussierten Indikationen und Technologieplattformen. Die ersten Gentherapien neuer Generation werden z.B. wohl nicht von Big Pharma auf den Markt gebracht werden. Wie die Übersicht in der Grafik 2 zeigt, lassen sich je nach Auswertungsfokus und Auswertungszeitpunkt über 350 Entwicklungsprojekte im Bereich der innovativen Therapien in Phase II und III finden.
Suche nach Opportunitäten
Eine der vielen Herausforderungen, die es für Big Pharma und etablierte Biotechunternehmen zu meistern gilt, wird darin liegen, im stagnierenden und preissensitiven makroökonomischen Umfeld die angestrebten Hochpreise für neue Therapien zu erzielen. Wie schwierig dies werden wird, zeigt die Preisentwicklung im (Massen)-Diabetesmarkt, aber auch bei der Behandlung bzw. sogar völligen Heilung von Hepatitis-C. Gesundheitssysteme werden vor allem dann, wenn sie gemeinschaftlich finanziert werden und geringe Wachstumsraten des gesamtwirtschaftlichen Systems nur geringe Einkommenszuwächse erlauben, an ihre Grenzen stoßen. Dies gilt umso mehr, wenn die Jahrestherapiekosten für Arzneimittel von relativ weit verbreiteten Krankheiten in die Hunderttausende gehen. Die Frage nach dem Wert der Innovationsleistung wird dann in vielen Fällen leider erst gar nicht gestellt. Auch scheint es im Moment schwierig, den Nettobarwert einer lebenslangen Therapie, samt seiner Kosten und Effekte auf das Gesamtsystem, gegen die Kosten einer kurzfristigen Therapie mit Heilung gegenzurechnen.
Für Big Pharma ergibt sich in der aktuellen Situation die Möglichkeit, im Rahmen einer strukturierten und gleichzeitig ergebnisoffenen Suche innovative und hochattraktive Entwicklungskandidaten außerhalb des strategischen Kernbereiches zu identifizieren. Aus der Sicht von Arthur D. Little liegen die Faktoren für eine erfolgreiche Suche und die dann folgende Umsetzung einer solchen, sog. White Space Strategie, insbesondere darin, die für das jeweilige Unternehmen am besten passenden Kandidaten zu selektieren. Dies bedeutet, die Vielzahl an Kandidaten mit den unternehmenseigenen Ansprüchen an z.B. pharmakologisches Risiko (Target und Pathway), Efficacy, Safety, Wettbewerbsintensität, Substitutionsgefahr und Market- Access-Hürden zu bewerten. Hinzu kommt, dass viele der attraktiven Kandidaten im Moment womöglich per se schon zu hoch bewertet sind.
Auswahl der Akquise-Kandidaten
Es läuft also alles auf die Kernfrage hinaus, wie große und mittlere Pharmafirmen mit ihren großen Kommerzialisierungspotenzialen in der Kombination von internen und externen Ressourcen effizient, nachvollziehbar und strukturiert die für sie richtigen von den falschen Akquise-Kandidaten unterscheiden können. Grundsätzlich gelingt es den meisten Business- Development-and-Licensing-Abteilungen mit den internen Ressourcen sehr gut, die bereits vorselektierten Kandidaten in den strategischen Kernbereichen zu bewerten. Unsere Erfahrung zeigt jedoch, dass externe Unterstützung speziell im Rahmen einer ergebnisoffenen Suche im White Space in drei Bereichen einen signifikanten Wertbeitrag in der Ergänzung zu den internen Ressourcen bringt.
Der erste Bereich umfasst die systematische und nachvollziehbare Aufbereitung der Kandidaten. Denn nicht selten gibt es viele Tausend Studien zu filtern und aufzubereiten. Je nachdem wie „früh" gesucht werden soll, werden entsprechend alle verfügbaren, neuen Entwicklungskandidaten in den klinischen Entwicklungsphasen I bis III ausgewählt. Bereits bekannte Therapiegebiete oder Therapiegebiete, welche bewusst als nicht passend definiert wurden, werden exkludiert. Ebenfalls ausgeschlossen werden Entwicklungskandidaten, die bereits mit den wichtigsten Pharmafirmen verbunden sind, bzw. in den Zielregionen nicht mehr verfügbar sind. Dieses Grundgerüst an Entwicklungskandidaten bildet den Raum für die detaillierte Suche und wird nun in mehreren Schritten und Interaktionen mit dem Auftraggeber von fachlichen Beraterteams auf ein überschaubares Maß an Kandidaten reduziert.
Der zweite Bereich liegt in der akademischen Flexibilität und Tiefe, die für ein solches Vorgehen notwendig sind. Da zu Beginn der Suche noch nicht in Gänze klar ist, in welchen Therapie- und Technologiegebieten eine wissenschaftliche Bewertung von Kandidaten zu erbringen sein wird, ist es meistens unmöglich, mit den firmeninternen Ressourcen seitens der Pharmafirmen diese Bewertung zu erbringen. Ein weltweit führendes, versatiles Netzwerk akademischer Spitzenkräfte ermöglicht es, innerhalb des Netzwerkes direkt oder im erweiterten Spektrum der bestehenden Kontakte sehr individuelle und beliebig spezifische Fragestellungen zu bearbeiten.
Der dritte Bereich ergibt sich aus der Tatsache, dass unter Zuhilfenahme eines externen Dienstleisters die Vertraulichkeit zu jeder Zeit gesichert bleibt. Auch kann es zu keinen Überschneidungen der Interessenlage in Hinblick auf Compliance kommen. Besteht nach erfolgreicher Identifikation attraktiver Kandidaten das Interesse, eine erste anonyme Ansprache zu starten, kann dies ebenfalls aus einer Hand angeboten werden.
Die Frage nach der Vermarktung
Für die Entwickler bzw. aktuellen Eigentümer an den Rechten der Pipelinekanditen stellt sich hingegen eine andere Frage: Soll der Kandidat auslizensiert werden oder geht man den Schritt der Vermarktung unter eigener Regie an? Oftmals ist es auch so, dass Biotechfirmen in der Vergangenheit bereits Kandidaten erfolgreich auslizensiert haben. Nach mehreren Jahren des erfolgreichen Wachstums und dem Aufbau und der Professionalisierung eigener Unternehmensstrukturen gilt es dann abzuwägen, ob und in welchen Märkten man den Schritt der Vermarktung selbst gehen möchte. Diese Entscheidung ist in jedem Falle individuell zu treffen.
Aus der Erfahrung von Arthur D. Little wird der Erfolg aber mit der Wahl für das richtige und „Fit-for-Purpose Commercial und Operational Model" entschieden. Hierzu gehören u.a. die Wahl des richtigen Vermarktungskanals in jedem Land, lokal angepasste Produktdifferenzierung, ein klares Verständnis über die Zulassungsprozesse und -sequenzen, die benötigten Informationen der Behörden, regulatorische Vorgaben für die Erstattungsentscheidung und Preisfindung, sowie eine Abwägung zwischen zentralen und dezentralen Distributionslösungen und die daraus resultierenden Niveaus an Transparenz und Kontrolle über die eigenen Produkte bis zum Endkunden. Da all diese Entscheidungen faktenbasiert und auf aktuellen Informationen getroffen werden sollten, empfiehlt es sich, großen Wert auf die Erhebung von Primärdaten zu legen und in jedem Markt zur Analyse der Erfolgsfaktoren mit lokalen und erfahrenen Teams zu arbeiten.
Kontakt
Arthur D. Little GmbH
Bernhard-Wicki-Str. 3
80636 München
Deutschland
+49 89/38088-700
+49 89/38088-750