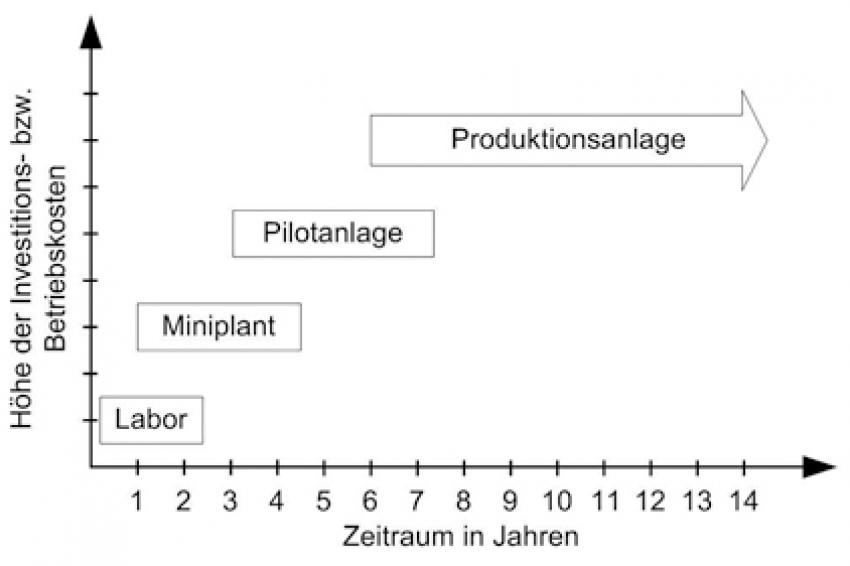
Die 50-Prozent-Idee: Vom Produkt zur Produktionsanlage in der Hälfte der Zeit
28.06.2012 -
CITplus - Die Chemische Industrie hat sich vorgenommen, die Zeit von der Produktidee zur laufenden Produktion um die Hälfte zu verkürzen.
Aufgrund gestiegener Ansprüche der Kunden, etwa in der Elektronik- oder der Automobilindustrie, ist derzeit eine Entwicklung in Richtung Spezialitätenchemie zu verzeichnen. Spezialchemikalien sind Produkte, die eher in kleineren Mengen bzw. Chargen hergestellt werden. Zudem können die Zyklen einzelner Produkte relativ kurz sein, kaum ist ein Produkt am Markt, soll es schon wieder durch einen Nachfolger abgelöst werden. Schnelligkeit zählt ganz besonders - Time is Money. Auch das Investitionsrisiko sinkt, wenn das Produkt rascher verkauft werden kann. Die übliche Dauer einer Prozessentwicklung kann gut und gerne um die 10 Jahre betragen, das ist für schnelllebige Produkte viel zu lang. Beim 48. Tutzing Symposion 2009 wurden diese Gedanken diskutiert und die Ergebnisse als „Thesen von Tutzing" zusammengefasst, die 50-Prozent-Idee war geboren.
Doppelt so schnell entwickeln, das ist leicht gesagt - aber weniger leicht getan. Gerade in den Bereichen Pharmaka und Spezialchemikalien sind die Herstellungsverfahren oft alles andere als simpel und erfordern eine Vielzahl zuweilen sehr komplexer Prozessschritte. Wie lässt sich der Entwicklungsprozess beschleunigen? Forscher in Firmen und Hochschulen arbeiten intensiv daran, die 50-Prozent-Idee mit Leben zu füllen.
Kontinuierlich dank Miniplant
Eine Möglichkeit, die Entwicklungsphase abzukürzen, sprechen Arno Behr von der TU Dortmund und sein Team an [2]: die konsequente Nutzung der Miniplant-Technologie. Ende der 1970er Jahre eingeführt, brachte sie enorme Fortschritte für die Prozessentwicklung. An der TU Dortmund wurden in den letzten Jahren verschiedene Miniplants aufgebaut, um im Labor entwickelte homogenkatalytische Batch-Reaktionen in kontinuierliche Prozesse zu überführen und auf technische Umsetzbarkeit hin zu untersuchen.
Miniplants sind meist Kleinanlagen im Technikumsmaßstab mit Volumina zwischen 0,5 und 5 l und Durchsätzen zwischen 0,01 kg/h-1 und 1 kg/h-1. Häufig lassen sich Minplants aus standardisiertem Laborequipment aufbauen. Aber auch wenn spezielle Apparate benötigt werden, können diese aufgrund der geringen Dimensionen kosten- und zeiteffektiv hergestellt werden. Miniplants lassen sich kontinuierlich betreiben. Das ist z. B. für katalytische Verfahren wichtig, um zuverlässige Aussagen über die Katalysatoraktivität im stationären Betriebszustand zu erhalten und um ein effektives Katalysatorrecycling auszuarbeiten. In einem Batch-Versuch kann zudem eine Rückführproblematik leicht übersehen werden: Geringe Verunreinigungen können sich nach 1.000 Rückführungen in einer kontinuierlichen Produktionsanlage zu Konzentrationen von 1 - 10 % akkumulieren.
Anders als Pilotanlagen sind Miniplants keine Produktionsanlagen en miniature. Stattdessen lassen sich verschiedenste Szenarien des späteren Prozesses ausprobieren. Miniplants werden in der Regel durch ein Prozessleitsystem kontrolliert, sodass anhand von Echtzeitanalysen ermittelt werden kann, wie der Prozess sich unter verschiedenen Bedingungen verhält. Mehrere potenzielle Verfahrensvarianten lassen sich, um Zeit zu sparen, parallel in verschiedenen Miniplants untersuchen.
Mit Miniplants sind, je nach Prozess, Scale-up-Faktoren von mehr 10.000 erreichbar. In manchen Fällen kann eine Maßstabsvergrößerung einer Miniplant direkt zur Produktionsanlage vollzogen werden.
Den Weg zum Fermentationsprozess beschleunigen
Nicht nur, aber auch wegen der beginnenden Energieversorgung mit Biotreibstoffen ist derzeit ein starker Biotrend zu verzeichnen. Viele bisher konventionelle Herstellungsverfahren werden auf biotechnologische Verfahren umgestellt. Entsprechend hoch ist der Bedarf an Werkzeugen zur schnellen und effizienten Entwicklung von Bioprozessen.
Effektive Fermentationsprozesse bilden die Basis für den Erfolg der modernen Biotechnologie. Aus zumeist Hunderten bis Tausenden von Klonen wird im ersten Schritt der beste Mikroorganismen-Stamm gesucht. Diese Tests erfolgen üblicherweise in Mikrotiterplatten. Beim anschließenden Sekundär-Screening wird, meist manuell in Schüttelkolben, die Performance eines Stammes unter verschiedenen Kultivierungsbedingungen (Medium, pH-Wert, Temperatur etc.) untersucht - mit entsprechend niedrigem Durchsatz.
In einem gemeinsamen Projekt der RWTH Aachen und der m2p-labs GmbH wurden Mikrotiterplatten mit blumenförmigen Wells, so genannte Flowerplates, und integrierter Online-Sensorik konzipiert, die Frank Kensy et al. im Themenheft der Chemie Ingenieur Technik vorstellen. Im Gegensatz zu konventionellen geschüttelten Mikrotiterplatten tritt bei diesem Design keine Sauerstofflimitierung auf. Mithilfe der Sensorik lassen sich bereits im Primär-Screening viele Erkenntnisse gewinnen, die sonst erst im Sekundär-Screening zugänglich wären. In manchen Fällen könnten die Schüttelkolbenversuche sogar ganz entfallen [3].
Mithilfe von Pipettierrobotern lassen sich die Versuche in den Flowerplates automatisieren. Zudem kann eine automatisierte Probennahme, Induktion, Fed-Batch-Prozessführung und pH-Nachjustierung erfolgen. So ließen sich zeit- und materialaufwendige Versuche in Laborfermentern einsparen und Bioprozesse hochparallel untersuchen. Da die großtechnischen Fermentationen meist als Fed-Batch-Verfahren laufen, liefern solche Tests unter Zufütterung von Nährstoffen zutreffendere Ergebnisse.
Das Rad nicht immer wieder neu erfinden: Modulare Ansätze
Ist es nötig, für einen neuen Prozess auch alle Apparate neu zu konzipieren? Nicht unbedingt. Voraussetzung für eine effiziente Wiederverwendung bewährter Lösungsmuster sind Modularisierung und Standardisierung, um zu gewerke- und lebensphasenübergreifenden, integrierten computergestützten Engineering-Prozessen zu gelangen. Am Lehrstuhl für Prozessleittechnik der TU Dresden werden Baukastensysteme zur Automatisierung modularer Anlagen an einer so genannten digitalen Modular Engineering & Automation Research (MEAR)-Anlage konzeptionell untersucht. Das Konzept der MEAR-Anlage sieht steckbare Prozessmodule vor, die jeweils mit einem eigenen Automatisierungssystem ausgestattet sind [4].
Leon Urbas et al. sehen aus Sicht der Prozessführung vor allem drei besondere Herausforderungen beim Thema Modularisierung:
Die für die Planung mit Konstruktionsmodulen notwendige Standardisierung führe unweigerlich zu einem höheren Instrumentierungsaufwand.
Die Automatisierung der Module müsse in ein Prozessführungskonzept integriert werden, das das gesamte System umfasst. Dies erfolge heute zumeist manuell und sei entsprechend fehleranfällig und zeitaufwendig.
Die Prozessführungskonzepte der einzelnen Module müssen derart gestaltet sein, dass aus den lokalen Führungsstrategien eine globale Führungsstrategie abgeleitet werden können.
Geld und Zeit sparen mit Wegwerfkomponenten?
Steckbare und standardisierte Bauteile sind ein interessanter Weg, wenn man diesen konsequent noch ein gutes Stück weiter geht, gelangt man zum Konzept der wegwerfbaren Komponenten. Einfache Disposables sind in Labor, Pilotanlage und Produktionsumfeld längst gängig, z. B. komplette, vorsterilisierte Benchtop-Bioreaktoren für den einmaligen Einsatz zur Verfahrensentwicklung im Liter-Maßstab. Inzwischen werden aber bereits ganze Pilot- oder Produktionsanlagen weitgehend auf der Basis von Disposable-Komponenten konzipiert - in der Hoffnung auf deutliche Zeit- und Kosteneinsparungen.
Helmut Brod und seine Co-Autoren von Bayer Technology Services bezweifeln, dass eine radikale Umsetzung des Disposable-Konzepts für alle Grundoperationen im Prozess per se zu einem technischen oder ökonomischen Optimalzustand führen könne. Hybridlösungen könnten dagegen ein sinnvoller Kompromiss für die Zukunft sein [5].
Disposable-Mischsysteme sind heute bis in den 5.000-Liter-Maßstab am Markt. Aufgrund der Verwendung von Polymerwerkstoffen für die Rührorgane sowie von Magnetkupplungen bleibt der volumenspezifische Leistungseintrag solcher Systeme allerdings vergleichsweise gering.
Bei den „Wegwerf-Bioreaktoren" beobachten die Autoren zwei Trends. Ein Teil der Hersteller versuche, mit den konstruktiven Mitteln der Disposable-Technologie den konventionellen Bioreaktoren so nahe wie möglich zu kommen, ein meist kostenintensiver Weg. Die andere Fraktion folge der Maxime, dass es weniger auf die Ähnlichkeit der Konstruktionen ankomme, sondern darauf, den Zellen eine definierte Mikroumgebung zur Verfügung zu stellen, etwa mithilfe unkonventioneller Agitations- und Begasungsprinzipien, wie dem Wippen der oberflächenbegasten Wave-Bioreaktoren oder der rotatorischen Oszillation der BaySHAKE-Bioreaktoren. Der Aufbau sei dann wesentlich einfacher und kostengünstiger umsetzbar.
Während Entwicklungen im Upstream-Bereich (Mischer und Bioreaktoren) fast zu Selbstläufern wurden und heute auch für Produktionsanlagen im Einsatz sind, läuft es im Downstream-Bereich nicht so rund: Grundoperationen wie die Ultrafiltration im Tangentialfluss oder auch die Säulenchromatographie seien noch nicht in entsprechenden Maßstäben verfügbar.
Anhand von Fallstudien demonstrieren die Autoren, dass eingesparte Investitionskosten durch erhöhte Produktionskosten über einen längeren Zeitraum der Anlage betrachtet schnell wett gemacht werden. Und die viel zitierte Beschleunigung von Investitionsprojekten? Sie gelinge nur dann, wenn die Single-use-Technologie konsequent eingesetzt werde, denn bei Hybridanlagen hängen Planungs- und Bauzeit an der Anschaffung der Langläufer-Komponenten und dem Aufwand für Installation und Verrohrung.
Probleme mit der Zuverlässigkeit mancher Disposables, mehr Handgriffe durch Bedienpersonal und benötigter Lagerraum für Vorratshaltung sowie regulatorischen Aspekte bei biopharmazeutischen Produkten sind weitere Nachteile.
Smart und flexibel: Milli-Reaktoren
Viele Spezialitäten werden in Rührkessel-Verfahren produziert - oft verschiedene Produkte batchweise in großen Apparaten. Bei kleinen Mengen oder unsicheren Markterwartungen ist dies alles andere als optimal. Aufgrund des sehr unterschiedlichen Apparateverhaltens im Labor-, Technikums-, Pilot- und Produktionsmaßstab ist das Scale-up von Rezepturen für den Rührkessel zudem schwierig und zeitaufwendig. „Smarte" Reaktorkonzepte wie Milli-Reaktoren könnten eine interessante Alternative darstellen, wie Stefan Lier von der Ruhr-Universität Bochum und seine Co-Autoren von der BASF SE anhand einer Wirtschaftlichkeitsanalyse darlegen [6].
Milli-Reaktoren sind kontinuierlich betriebene Apparate mit Strömungskanälen im Millimeterbereich, z. B. Hochleistungs-Mischer-Wärmeaustauscher-Reaktoren. Diese Apparate bieten um mehrere Größenordnungen höhere Wärmeaustauscherflächen pro Volumeneinheit als klassische Rührkessel. Anders als Mikro-Reaktoren haben sie wegen ihrer größeren Abmessungen kaum mit Verstopfungen zu kämpfen. Reaktionen lassen sich unter sehr scharfen Bedingungen fahren und exakt steuern. So eröffnen sich ein erweitertes Prozessfenster und Möglichkeiten zur gezielten Einstellung von Produkteigenschaften bei der Produktentwicklung. Hochleistungs-Mischer-Wärmeaustauscher-Reaktoren lassen sich wesentlich einfacher über einen größeren Durchsatzbereich hochskalieren als Rührkessel. Sie sind aus kompakten, standardisierten und vorgefertigten Komponenten rasch aufbaubar. Ein weiterer Vorteil: Es können Anlagenmodule für kleine Kapazitäten gebaut und die Anlagenkapazität durch Parallelisierung der Anlagenmodule erhöht werden. So lassen sich Produktionskapazitäten einfacher an die aktuelle Marktnachfrage anpassen.
Hochskalieren mikro-strukturierter Apparate
Das Hochskalieren, also die Erhöhung der Durchsatzmenge oder der Produktionskapazität eines chemischen Prozesses unter vergleichbaren Prozessbedingungen, ist ein entscheidender Faktor bei der Prozessentwicklung. Oben wurde dieser Aspekt bereits für Rührkessel diskutiert und Alternativen aufgezeigt. Norbert Kockmann von der TU Dortmund berichtet im 50-Prozent-Idee-Themenheft der CIT über den Einsatz und die Scale-up-Strategie von kontinuierlich betriebenen mikrostrukturierten und konventionellen Rohrreaktoren [7].
Kontinuierlich betriebene Strömungsreaktoren mit mikrostrukturierten Elementen haben ihren Platz gefunden für die Prozessentwicklung im Labor und für die weitere Entwicklung sowie die Kleinmengenproduktion im Pilotmaßstab. Im Gegensatz zu einzelnen mikrostrukturierten Elementen wie individuellen Mikromischern erlaubt der modularisierte Mikroreaktor die Integration von mehreren Funktionen, z. B. können Vermischen und Wärmeaustausch mit Verweilmodulen kombiniert werden, um die Reaktorleistung zu optimieren. Ein Beispiel ist der FlowPlate Plattenreaktor von Lonza (siehe Abb. 4).
Ein Schlüsselfaktor beim Reaktor-Scale-up ist die spezifische Kanalanordnung mit Misch- und Verweilzeit-Segmenten, die eine geometrische Ähnlichkeit über die gesamte Längenskala haben. Mithilfe dimensionsloser Kennzahlen und kinetischer Parameter gelingt auch bei exothermen Reaktionen ein sicheres Hochskalieren mit verändertem Wärmeübergang. Dies wird durch modular aufgebaute Apparate erleichtert, die mithilfe einer Plattformstrategie auf verschiedenen Niveaus des Durchsatzes oder anderer Prozessparameter konzipiert werden.
Für das Sicherheitskonzept gefährlicher Reaktionen müssen außer dem Reaktor auch Pumpen, Auffangbehälter und eventuelle Trennoperationen bei der Prozessentwicklung und dem Hochskalieren genau betrachtet werden [8]. So können Reagenzien z. B. durch Pumpenfehler schon im Zulauf in Kontakt kommen, oder eine unvollständige Reaktion im Mikroreaktor kann zu Problemen im Reaktorauslass führen.
Anhand von Beispielreaktionen erläutert Kockmann sicherheitstechnische Maßnahmen bei Mikroreaktoren. Dabei helfen die HAZOP-Methode (Hazard and Operability) und andere im Anlagenbau etablierte Maßnahmen zur Festlegung und Überprüfung von Sicherheitsmaßnahmen sowie Checklisten zur Prozess- und Arbeitssicherheit. Für die Zukunft sei es wichtig, weitere Erfahrungen aus dem Produktionseinsatz mikrostrukturierter Apparate zu generieren und in die Diskussion einzubringen, um mehr Vertrauen in deren Robustheit zu gewinnen.
Literatur
[1] Editorial CIT
[2] Arno Behr, Henning Witte und Michael Zagajewski: Scale-up durch Miniplant-Technik: Anwendungsbeispiele aus der homogenen Katalyse; DOI: 10.1002/cite.201100169
Prof. Dr. Arno Behr, Technische Universität Dortmund
[3] Pamela Wenk, Johannes Hemmerich, Carsten Müller und Frank Kensy: Hochparallele Bioprozessentwicklung in geschüttelten Mikrobioreaktoren; DOI: 10.1002/cite.201100206
Dr.-Ing. Frank Kensy, m2p-labs GmbH, Baesweiler; kensy@m2p-labs.com
[4] Leon Urbas, Falk Doherr, Annett Krause und Michael Obst: Modularisierung und Prozessführung; DOI: 10.1002/cite.201200034
Prof. Dr.-Ing. Leon Urbas, Technische Universität Dresden; leon.urbas@tu-dresden.de
[5] Helmut Brod, Andrea Vester und Jörg Kauling: Möglichkeiten und Grenzen von Disposable-Technologien in biopharmazeutischen Verfahren; DOI: 10.1002/cite.201100229
Dr.-Ing. Helmut Brod, Bayer Technology Services GmbH, Leverkusen; helmut.brod@bayer.com
[6] Andreas Brodhagen, Marcus Grünewald, Matthias Kleiner und Stefan Lier: Erhöhung der Wirtschaftlichkeit durch beschleunigte Produkt- und Prozessentwicklung mit Hilfe modularer und skalierbarer Apparate; DOI: 10.1002/cite.201100220
Stefan Lier, Ruhr-Universität Bochum; Lier@fluidvt.rub.de
[7] Norbert Kockmann: Scale-up-fähiges Equipment für die Prozessentwicklung; DOI: 10.1002/cite.201100218
Prof. Dr. Norbert Kockmann, Technische Universität Dortmund; norbert.kockmann@bci.tu-dortmund.de
[8] Norbert Kockmann: Sicherheitsaspekte bei der Prozessentwicklung und Kleinmengenproduktion mit Mikroreaktoren; DOI: 10.1002/cite.201100222
Dr. Kristin Mädefessel-Herrmann,
freie Wissenschaftsjournalistin